ADVERTISEMENT
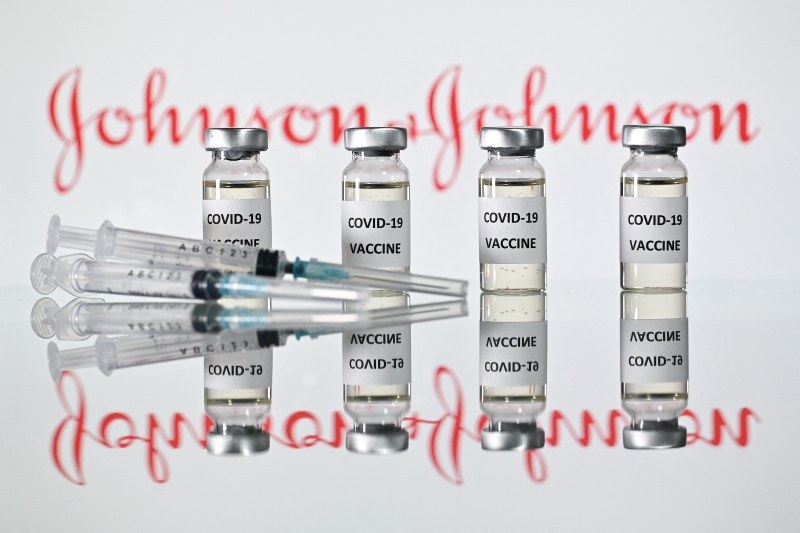
(亚特兰大28日综合电)美国食品及药物管理局(FDA)上周六正式批准授权庄生疫苗的紧急使用,它成为第三种在美国获批使用的冠病疫苗,也是美国首个单针接种的冠病疫苗。
庄生公司早前指,最快可于当地周一提供疫苗,首批约300至400万剂,预期3月底,能提供足够2000万人接种的剂量。
庄生公司已承诺在6月底前向美国政府提供1亿剂疫苗。结合辉瑞和莫德纳承诺的7月底前提供6亿剂,意味着足够让每个想要注射疫苗的美国人都能获取。
庄生疫苗用重组腺病毒作为载体,只需接种一剂就可以产生抗体,整体有效率66.1%。庄生早前向美国食药局提交来自8个国家、4.4万名参与者的临床试验数据,显示在美国,这种疫苗预防中度至重度病征的有效率为72%,在出现变种病毒的南非则跌至64%。在不同国家,接种疫苗1个月后,已可完全预防住院和死亡。
ADVERTISEMENT
热门新闻





百格视频





ADVERTISEMENT