


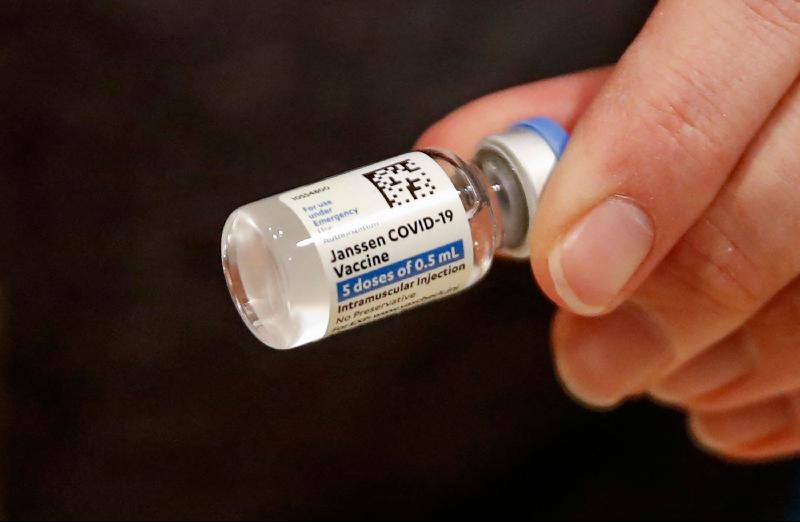
(华盛顿1日综合电)《纽约时报》报道,马里兰州巴尔的摩一间生产冠病疫苗的工厂,有工人数周前意外将用于生产阿斯利康疫苗及庄生疫苗的原料搞混,导致1500万剂庄生疫苗报废,这对庄生加快提高产量造成打击。
根据报道,这座工厂与庄生和英国阿斯利康公司合作生产疫苗,事件迫使监管机关延后批准对工厂生产线的许可。
ADVERTISEMENT
官员认为是人为错误,食品及药物管理局(FDA)正调查事件,工厂要暂停庄生疫苗出货,以确保疫苗安全,预计会影响美国原定下月付运的数以千万剂庄生疫苗,但不会影响美国正在使用的批次。
庄生回应法新社询问时表示,已发现Emergent BioSolutions制药公司经营的一间巴尔的摩工厂,有一批疫苗“未达品质标准”,但没有证实受波及的确切数量。
庄生强调,这批疫苗“从未进入制造程序的填充和完成阶段,维持品质与安全仍是我们的首要之务”。
但《纽时》指出,品质管控问题可能影响未来产量,预料FDA将加以调查。FDA “知道这个状况”,但不愿进一步评论。
庄生表示,将派更多专家到工厂“监督、指导与支援所有庄生COVID-19疫苗的制造过程”,以便于4月再交付2400万剂疫苗。
Emergent BioSolutions说,这座工厂尚未获美国监管机关授权制造庄生疫苗“药剂”;但美媒报道,工厂预计在不久的将来生产数以千万剂。
庄生疫苗因为仅须施打一剂而广获赞赏,且不像莫德纳与辉瑞疫苗需要冷冻保存,这让配送变得更简单。
庄生说:“我们持续预计将在2021年年底前交付超过10亿剂COVID-19疫苗。”
官员预期现时的疫苗数量仍可达到总统拜登在5月底前,为所有成年人接种的目标,辉瑞和莫德纳药厂仍然继续供应疫苗。
ADVERTISEMENT
热门新闻





百格视频





ADVERTISEMENT


































